Обзор
Быстрая идентификация трансгенных растений
Текст/Тун Юйчэн
Экспериментальная операция/Хань Ин
Редактор/Вэнь Юджун
Слов/1600+
Рекомендуемое время чтения/8-10 минут
Быстрая идентификация трансгенных растений
Новичку в лаборатории не стоит отсеивать положительные растения из группы растений с низкой конверсией.Во-первых, ДНК нужно выделять из большого количества образцов один за другим, а затем методом ПЦР выявлять чужеродные гены.Однако результаты часто представляют собой пробелы и полосы, иногда с несколькими элементами, но невозможно определить, есть ли пропущенные обнаружения или ложные обнаружения..Это очень беспомощно перед таким экспериментальным процессом и результатами?Не волнуйтесь, брат научит вас легко и точно отсеивать трансгенные положительные растения.
Шаг 1: Праймеры для обнаружения дизайна
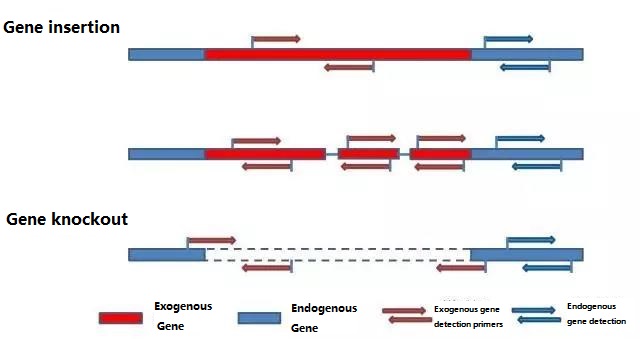
Определите эндогенный ген и экзогенный ген, которые необходимо обнаружить, в соответствии с тестируемым образцом и выберите репрезентативную последовательность 100-500 п.н. в гене для дизайна праймера.Хорошие праймеры могут обеспечить точность результатов обнаружения и сократить время обнаружения (см. приложение для часто используемых праймеров для обнаружения).
Примечание:
Недавно разработанные праймеры должны оптимизировать условия реакции и проверить правильность, прецизионность и предел обнаружения перед выполнением крупномасштабного обнаружения.
Шаг 2:Разработать экспериментальный протокол

Положительный контроль: используйте очищенную ДНК, содержащую целевой фрагмент, в качестве матрицы, чтобы определить, являются ли реакционная система и условия ПЦР нормальными.
Отрицательный/пустой контроль: Используйте матрицу ДНК или ddH.2O, не содержащий целевой фрагмент, в качестве матрицы для определения наличия источника загрязнения в системе ПЦР.
Внутренний эталонный контроль: используйте комбинацию праймер/зонд эндогенного гена тестируемого образца, чтобы оценить, может ли матрица быть обнаружена с помощью ПЦР.
Примечание:
Положительные, отрицательные/пустые контроли и контроли внутреннего контроля должны быть установлены для каждого теста, чтобы оценить достоверность экспериментальных результатов.
Шаг 3: Подготовка эксперимента

Перед использованием наблюдайте, равномерно ли перемешан раствор.При обнаружении осадка перед применением его нужно растворить и перемешать согласно инструкции.Смесь 2×PCR необходимо пипетировать и многократно смешивать с помощью микропипетки перед использованием, чтобы избежать неравномерного распределения ионов.
Примечание:
Достаньте инструкции и внимательно прочитайте их, и сделайте приготовления перед экспериментом в строгом соответствии с инструкциями.
Шаг 4: Подготовьте реакционную систему ПЦР
Согласно экспериментальному протоколу, смешайте праймеры, H2O, смесь 2×ПЦР, центрифугировать и распределить по каждой реакционной пробирке.
Примечание:
Для крупномасштабных или долгосрочных испытаний рекомендуется использовать реакционную систему ПЦР, содержащую фермент UNG, который может эффективно избежать аэрозольного загрязнения, вызванного продуктами ПЦР.
Шаг 5. Добавьте шаблон реакции

Используя технологию прямой ПЦР, нет необходимости в утомительном процессе очистки нуклеиновых кислот.Матрица образца может быть подготовлена в течение 10 минут и добавлена в соответствующую реакционную систему ПЦР.
Примечание:
Метод лизиса имеет лучший эффект детекции, а полученный продукт можно использовать для множественных реакций детекции.
5.1: Прямая ПЦР листьев
В соответствии с размером рисунка в руководстве нарежьте ткань листа диаметром 2-3 мм и поместите ее в реакционную систему ПЦР.
Примечание. Убедитесь, что фрагменты листьев полностью погружены в раствор реакции ПЦР, и не добавляйте чрезмерную ткань листьев.
5.2: Метод лизиса листьев
Вырежьте ткань листа диаметром 5-7 мм и поместите ее в центрифужную пробирку.Если вы выбираете зрелые листья, избегайте использования тканей основной жилки листа.Внесите пипеткой 50 мкл лизата буфера P1 в центрифужную пробирку, чтобы убедиться, что лизат может полностью погрузить ткань листа, поместите его в термоциклер или металлическую баню и лизируйте при 95°C в течение 5-10 минут.


Добавьте 50 мкл нейтрализующего раствора Buffer P2 и хорошо перемешайте.Полученный лизат можно использовать в качестве матрицы и добавить в реакционную систему ПЦР.
Примечание. Количество матрицы должно составлять от 5 до 10 % системы ПЦР и не должно превышать 20 % (например, в систему ПЦР на 20 мкл добавьте 1–2 мкл буфера для лизиса, но не более 4 мкл).
Шаг 6: реакция ПЦР

После центрифугирования реакционной пробирки для ПЦР поместите их в прибор для ПЦР для амплификации.
Примечание:
В реакции используется неочищенная матрица для амплификации, поэтому количество циклов амплификации на 5-10 циклов больше, чем при использовании очищенной ДНК-матрицы.
Шаг 7: Обнаружение электрофореза и анализ результатов

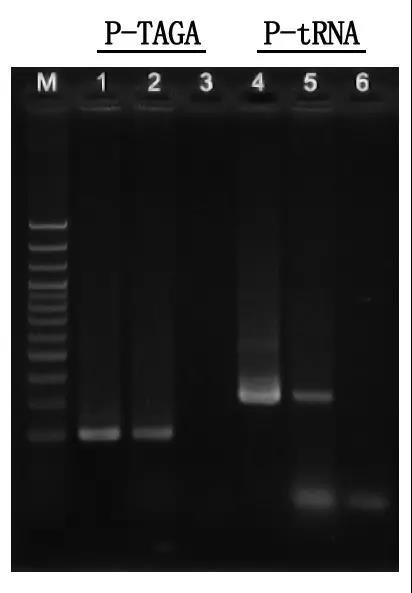
M: лестница ДНК 100 п.н.
1\4: Метод очищенной ДНК
2\5: прямой метод ПЦР
3\6: Пустой элемент управления
Контроль качества:
Результаты испытаний различных контролей, установленных в эксперименте, должны соответствовать следующим условиям.В противном случае следует проанализировать причину проблемы и повторно выполнить тест после устранения проблемы.
Таблица 1. Нормальные результаты тестов различных контрольных групп

* Когда плазмида используется в качестве положительного контроля, результат теста эндогенного гена может быть отрицательным.
Результат решения:
A. Результат теста эндогенного гена образца отрицательный, что указывает на то, что ДНК, пригодная для обычной ПЦР-детекции, не может быть извлечена из образца или выделенная ДНК содержит ингибиторы реакции ПЦР, и ДНК следует экстрагировать снова.
B. Результат теста эндогенного гена образца положительный, а результат теста экзогенного гена отрицательный, что указывает на то, что ДНК, пригодная для обнаружения с помощью обычной ПЦР, извлечена из образца, и можно судить, что ген XXX в образце не обнаружен.
C. Результат теста эндогенного гена образца положительный, а результат теста экзогенного гена положительный, что указывает на то, что ДНК, подходящая для обычной ПЦР-детекции, была извлечена из образца, а ДНК образца содержит ген XXX.В дальнейшем могут быть проведены подтверждающие эксперименты.
Шаг 8: Разработка праймеров для обнаружения

После эксперимента используйте 2% раствор гипохлорита натрия и 70% раствор этанола, чтобы протереть экспериментальную зону, чтобы предотвратить загрязнение окружающей среды.
Приложение
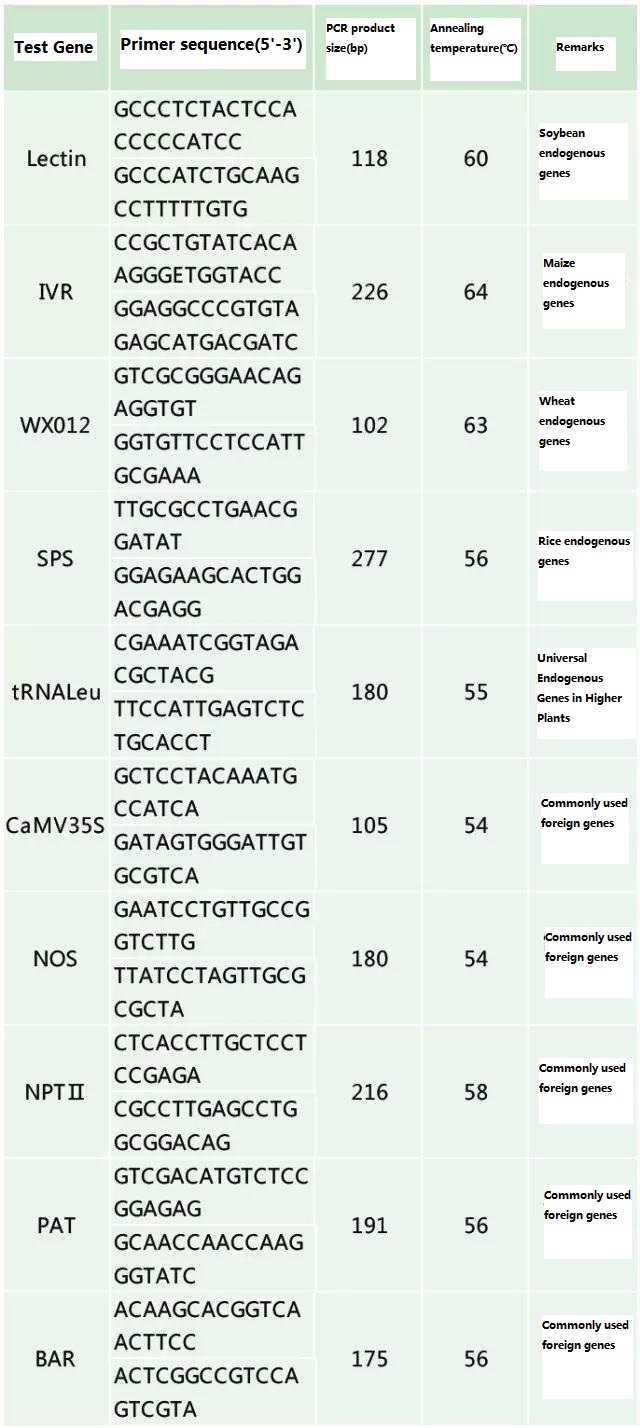
Таблица 2. Обычно используемые праймеры для общей ПЦР-детекции генетически модифицированных растений
Справочный документ:
СН/Т 1202-2010, Метод качественной ПЦР для выявления генетически модифицированных растительных ингредиентов в пищевых продуктах.
Объявление Министерства сельского хозяйства 1485-5-2010, Тестирование ингредиентов генетически модифицированных растений и продуктов из них - риса М12 и его производных.
Время публикации: 09 июня 2021 г.








