Технология молекулярной диагностики использует методы молекулярной биологии для определения экспрессии и структуры генетического материала человеческого тела и различных патогенов, чтобы достичь цели прогнозирования и диагностики заболеваний.
В последние годы, с модернизацией и повторением технологии молекулярной диагностики, клиническое применение молекулярной диагностики становится все более и более обширным и глубоким, и рынок молекулярной диагностики вступил в период быстрого развития.
Автор суммирует распространенные на рынке технологии молекулярной диагностики и делится на три части: в первой части представлена технология ПЦР, во второй части представлена технология изотермической амплификации нуклеиновых кислот, а во второй части представлена технология секвенирования.
01
Часть I: технология ПЦР
технология ПЦР
ПЦР (полимеразная цепная реакция) — одна из технологий амплификации ДНК in vitro, история которой насчитывает более 30 лет.
Технология ПЦР была впервые применена в 1983 году Кэри Маллисом из Цетуса, США.Маллис подал заявку на патент ПЦР в 1985 году и в том же году опубликовал первую научную статью о ПЦР.Маллис получил Нобелевскую премию по химии в 1993 году.
Основные принципы ПЦР
ПЦР может амплифицировать целевые фрагменты ДНК более чем в миллион раз.Принцип заключается в том, что при катализе ДНК-полимеразой в качестве матрицы используется исходная цепь ДНК, а в качестве отправной точки для удлинения используется специфический праймер.Он реплицируется in vitro с помощью таких этапов, как денатурация, отжиг и удлинение.Процесс комплементарности дочерней цепи ДНК матричной ДНК родительской цепи.
Стандартный процесс ПЦР делится на три этапа:
1. Денатурация: используйте высокую температуру для разделения двойных цепей ДНК.Водородные связи между двойными цепями ДНК разрываются при высоких температурах (93-98°С).
2. Отжиг: после разделения двухцепочечной ДНК температуру понижают, чтобы праймер мог связываться с одноцепочечной ДНК.
3. Удлинение: ДНК-полимераза начинает синтезировать комплементарные цепи вдоль цепей ДНК из связанных праймеров при понижении температуры.Когда удлинение завершено, цикл завершается, и количество фрагментов ДНК удваивается.
Повторяя эти три шага 25-35 раз, количество фрагментов ДНК будет увеличиваться в геометрической прогрессии.
Изобретательность ПЦР заключается в том, что для разных генов-мишеней можно создавать разные праймеры, так что фрагменты генов-мишеней могут быть амплифицированы за короткий период времени.
Пока что ПЦР можно разделить на три категории, а именно обычную ПЦР, флуоресцентную количественную ПЦР и цифровую ПЦР.
Первое поколение обычной ПЦР
Используйте обычный инструмент для амплификации ПЦР для амплификации гена-мишени, а затем используйте электрофорез в агарозном геле для обнаружения продукта, можно провести только качественный анализ.
Основные недостатки ПЦР первого поколения:
-Склонен к неспецифической амплификации и ложноположительным результатам.
- Обнаружение занимает много времени, а операция громоздка.
-Только качественное тестирование может быть сделано.
Флуоресцентная количественная ПЦР второго поколения
Количественная флуоресцентная ПЦР (ПЦР в реальном времени), также известная как кПЦР, используется для мониторинга накопления амплифицированных продуктов путем накопления флуоресцентных сигналов путем добавления флуоресцентных зондов, которые могут указывать на ход реакционной системы, и для оценки результатов по кривой флуоресценции, и ее можно количественно определить с помощью значения Cq и стандартной кривой.
Поскольку технология кПЦР осуществляется в закрытой системе, снижается вероятность контаминации, а сигнал флуоресценции можно контролировать для количественного определения, поэтому она наиболее широко используется в клинической практике и стала доминирующей технологией в ПЦР.
Флуоресцентные вещества, используемые в количественной флуоресцентной ПЦР в реальном времени, можно разделить на: флуоресцентные зонды TaqMan, молекулярные маяки и флуоресцентные красители.
1) Флуоресцентный зонд TaqMan:
Во время ПЦР-амплификации добавляется специфический флуоресцентный зонд при добавлении пары праймеров.Зонд представляет собой олигонуклеотид, и два его конца помечены соответственно репортерной флуоресцентной группой и флуоресцентной группой гасителя.
Когда зонд не поврежден, флуоресцентный сигнал, испускаемый репортерной группой, поглощается гасящей группой;во время ПЦР-амплификации 5'-3'-экзонуклеазная активность фермента Taq расщепляет и разрушает зонд, в результате чего репортерная флуоресцентная группа и гаситель флуоресцентной группы разделяются, так что система мониторинга флуоресценции может получать флуоресцентный сигнал, то есть каждый раз, когда амплифицируется нить ДНК, образуется флуоресцентная молекула, а накопление флуоресцентного сигнала полностью синхронизируется с образованием продукта ПЦР.
2) флуоресцентные красители SYBR:
В реакционную систему ПЦР добавляют избыток флуоресцентного красителя SYBR.После того, как флуоресцентный краситель SYBR неспецифически встраивается в двойную цепь ДНК, он излучает флуоресцентный сигнал.Молекула красителя SYBR, не включенная в цепь, не будет излучать никакого флуоресцентного сигнала, тем самым обеспечивая флуоресцентный сигнал. Увеличение продуктов ПЦР полностью синхронизировано с увеличением продуктов ПЦР.SYBR связывается только с двухцепочечной ДНК, поэтому кривую плавления можно использовать для определения специфичности реакции ПЦР.
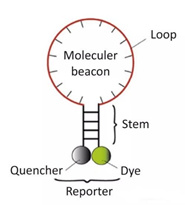
3) Молекулярные маяки
Это олигонуклеотидный зонд с двойной меткой «стебель-петля», который образует структуру шпильки примерно из 8 оснований на 5-м и 3-м концах.Последовательности нуклеиновых кислот на обоих концах комплементарно спарены, в результате чего флуоресцентная группа и группа гашения являются плотными.Закройте, он не будет производить флуоресценцию.
После получения продукта ПЦР в процессе отжига средняя часть молекулярного маяка соединяется с определенной последовательностью ДНК, а флуоресцентный ген отделяется от гена гасителя для получения флуоресценции.
Основные недостатки ПЦР второго поколения:
Чувствительность по-прежнему недостаточна, а обнаружение малокопийных экземпляров не является точным.
Существует влияние фонового значения, и результат чувствителен к помехам.
Цифровая ПЦР третьего поколения
Цифровая ПЦР (DigitalPCR, dPCR, Dig-PCR) рассчитывает количество копий целевой последовательности посредством определения конечной точки и может выполнять точное абсолютное количественное определение без использования внутренних контролей и стандартных кривых.
Цифровая ПЦР использует определение конечной точки и не зависит от значения Ct (порога цикла), поэтому на реакцию цифровой ПЦР меньше влияет эффективность амплификации, а устойчивость к ингибиторам реакции ПЦР улучшается с высокой точностью и воспроизводимостью.
Благодаря характеристикам высокой чувствительности и высокой точности, ингибиторы реакции ПЦР не мешают ему, и он может обеспечить истинную абсолютную количественную оценку без стандартных продуктов, что стало горячей точкой исследований и приложений.
В соответствии с различными формами реакционного блока его можно разделить на три типа: микрожидкостные, чиповые и капельные системы.
Время публикации: 08 июля 2021 г.