Исходный материал: РНК
Количественная ПЦР с обратной транскрипцией (RT-qPCR) представляет собой экспериментальный метод, используемый в экспериментах с ПЦР с использованием РНК в качестве исходного материала.В этом методе общая РНК или информационная РНК (мРНК) сначала транскрибируется в комплементарную ДНК (кДНК) с помощью обратной транскриптазы.Затем проводили реакцию количественной ПЦР с использованием кДНК в качестве матрицы.RT-qPCR использовался в различных приложениях молекулярной биологии, включая анализ экспрессии генов, проверку интерференции РНК, проверку микрочипов, обнаружение патогенов, генетическое тестирование и исследование заболеваний.
Одноэтапные и двухэтапные методы RT-qPCR
RT-qPCR можно выполнять одноэтапным или двухэтапным методом.Одноэтапная RT-qPCR сочетает в себе обратную транскрипцию и ПЦР-амплификацию, позволяя обратной транскриптазе и ДНК-полимеразе завершить реакцию в одной и той же пробирке в одних и тех же буферных условиях.Одноэтапная RT-qPCR требует использования только специфичных для последовательности праймеров.В двухэтапной RT-qPCR обратная транскрипция и ПЦР-амплификация выполняются в двух пробирках с использованием разных оптимизированных буферов, условий реакции и стратегий дизайна праймеров.
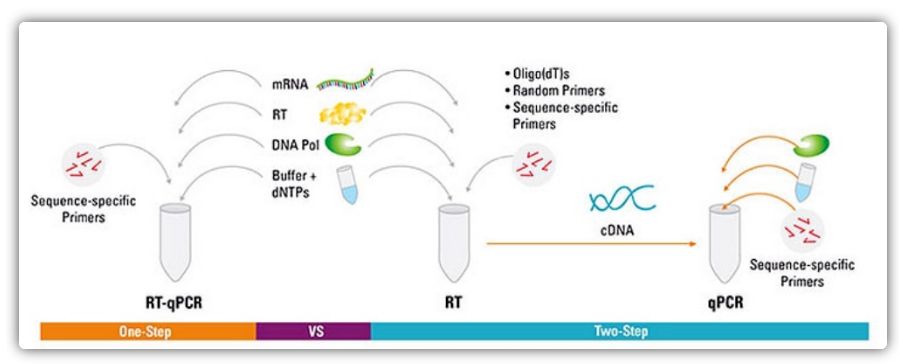
| Преимущество | Недостаток | |
| Один шаг | Этот метод имеет меньшую экспериментальную ошибку, так как обе реакции проводятся в одной пробирке.
Меньшее количество шагов пипетирования снижает риск загрязнения
Подходит для высокопроизводительного амплификации/скрининга, быстро и воспроизводимо | Двухстадийные реакции не могут быть оптимизированы отдельно
Поскольку условия реакции ухудшаются при объединении двухстадийной реакции, чувствительность не так хороша, как у двухстадийного метода.
Количество целей, обнаруженных одним образцом, невелико |
| Два шага | Возможность создания стабильных библиотек кДНК, которые можно хранить в течение длительного периода времени и использовать в различных реакциях.
Гены-мишени и эталонные гены могут быть амплифицированы из одной и той же библиотеки кДНК без необходимости использования нескольких библиотек кДНК.
Реакционные буферы и условия реакции, которые позволяют оптимизировать прогоны одной реакции
Гибкий выбор условий запуска | Использование нескольких пробирок и большее количество шагов пипетирования увеличивает риск загрязнения ДНК. и занимает много времени.
Требует большей оптимизации, чем одношаговый метод |
Сопутствующие товары:
RT-qPCR Easyᵀᴹ (One Step)-SYBR Green I
RT-qPCR Easyᵀᴹ (One Step)-Taqman
RT Easyᵀᴹ I Master Premix для синтеза первой цепи CDNA
ПЦР в реальном времени Easyᵀᴹ-SYBR Green I Kit
ПЦР в реальном времени Easyᵀᴹ-Taqman
Отбор тотальной РНК и мРНК
При разработке эксперимента RT-qPCR важно решить, использовать ли общую РНК или очищенную мРНК в качестве шаблона для обратной транскрипции.Хотя мРНК может обеспечить несколько более высокую чувствительность, общая РНК по-прежнему часто используется.Причина этого в том, что тотальная РНК как исходный материал имеет более важное преимущество, чем мРНК.Во-первых, процесс требует меньшего количества стадий очистки, что обеспечивает лучшее количественное извлечение матрицы и лучшую нормализацию результатов к исходным числам клеток.Во-вторых, он позволяет избежать этапа обогащения мРНК, что позволяет избежать возможности искажения результатов из-за разного восстановления разных мРНК.В целом, поскольку в большинстве приложений относительная количественная оценка целевого гена более важна, чем абсолютная чувствительность обнаружения, в большинстве случаев больше подходит тотальная РНК.
Праймер обратной транскрипции
В двухэтапном методе можно использовать три разных метода для праймирования реакции кДНК: олиго(dT) праймеры, случайные праймеры или праймеры, специфичные для последовательности.Как правило, олиго(dT) праймеры и случайные праймеры используются в комбинации.Эти праймеры отжигаются на матричной цепи мРНК и обеспечивают обратную транскриптазу отправной точкой для синтеза.
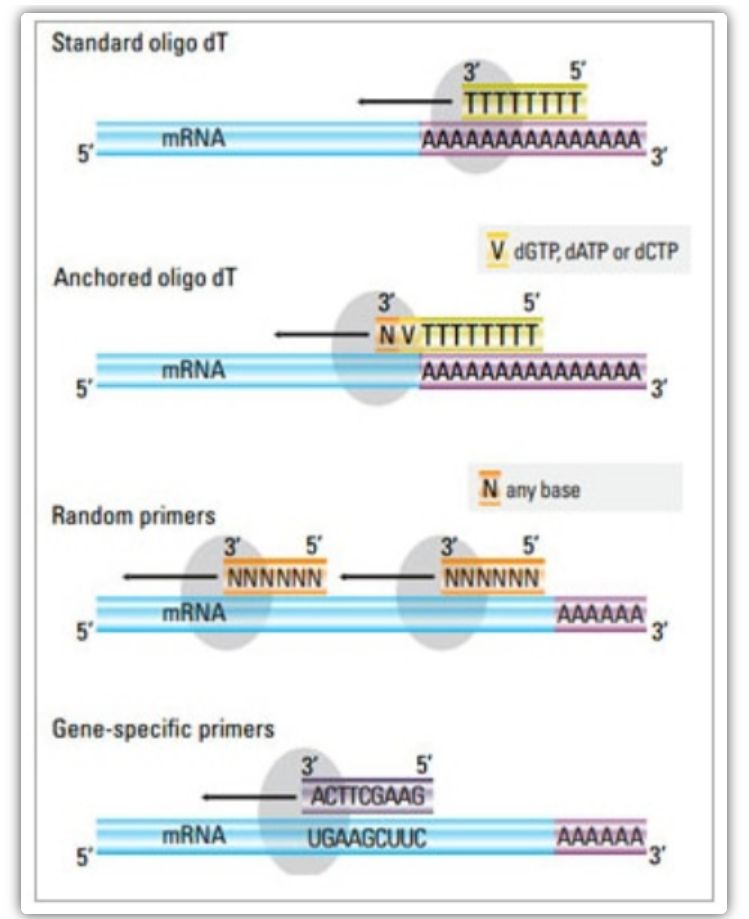
| Выбор грунтовки | Структура и функция | Преимущество | Недостаток |
| Олиго(dT) праймер (или закрепленный олиго(dT) праймер) | Расширенный отжиг до остатков тимина на поли(А)-хвосте мРНК;якорный олиго(dT) праймер содержит G, C или A на 3'-конце (якорный сайт) | Синтез полноразмерной кДНК из мРНК с поли(А)-хвостом
Применяется, когда доступно меньше исходного материала
Якорный сайт гарантирует, что олиго(dT) праймер связывается с 5'-поли(А) хвостом мРНК. | Подходит только для амплификации генов с поли(А)-хвостами
Получите кДНК, усеченную от сайта праймирования*2 в поли(А)
Склонен к связыванию с 3'-концом*
*Эта возможность сводится к минимуму, если используются закрепленные олиго(dT) праймеры. |
| случайный праймер
| Длина от 6 до 9 оснований, которые могут отжигаться на нескольких сайтах во время транскрипции РНК. | Отжиг ко всем РНК (тРНК, рРНК и мРНК)
Подходит для транскриптов со значительной вторичной структурой или когда доступно меньше исходного материала
Высокий выход кДНК | кДНК подвергается обратной транскрипции со всей РНК, что обычно нежелательно и может ослабить сигнал мРНК-мишени.
получить укороченную кДНК |
| праймеры, специфичные для последовательности | Пользовательские праймеры, нацеленные на определенные последовательности мРНК | специфическая библиотека кДНК
Улучшить чувствительность
Использование обратных праймеров для количественной ПЦР | Ограничено только синтезом одного гена-мишени |
Обратная транскриптаза
Обратная транскриптаза — это фермент, использующий РНК для синтеза ДНК.Некоторые обратные транскриптазы обладают РНКазной активностью и могут разрушать цепи РНК в гибридных цепях РНК-ДНК после транскрипции.Если он не обладает ферментативной активностью РНКазы, можно добавить РНКазу Н для повышения эффективности количественной ПЦР.Обычно используемые ферменты включают обратную транскриптазу вируса мышиного лейкоза Молони и обратную транскриптазу вируса миелобластомы птиц.Для RT-qPCR идеально выбирать обратную транскриптазу с более высокой термостабильностью, чтобы синтез кДНК можно было проводить при более высоких температурах, обеспечивая успешную транскрипцию РНК с более высокой вторичной структурой, сохраняя при этом их полную активность на протяжении всей реакции, что приводит к более высоким выходам кДНК.
Сопутствующие товары:
Обратная транскриптаза Foreasy M-MLV
РНКаза H активность обратной транскриптазы
РНКаза Н способна расщеплять нити РНК из дуплексов РНК-ДНК, обеспечивая эффективный синтез двухцепочечной ДНК.Однако при использовании длинной мРНК в качестве матрицы РНК может преждевременно расщепляться, что приводит к укорочению кДНК.Поэтому часто полезно минимизировать активность РНКазы Н во время клонирования кДНК, если желателен синтез длинных транскриптов.Напротив, обратные транскриптазы с активностью РНКазы H часто полезны для приложений количественной ПЦР, поскольку они усиливают плавление дуплексов РНК-ДНК во время первого цикла ПЦР.
Дизайн грунтовки
Праймеры ПЦР, используемые для этапа количественной ПЦР в ОТ-КПЦР, в идеале должны быть разработаны так, чтобы охватывать экзон-экзонное соединение, где праймер для амплификации потенциально может охватывать фактическую границу экзон-интрон.Поскольку последовательности геномной ДНК, содержащие интроны, не амплифицируются, этот дизайн снижает риск ложноположительных результатов, амплифицированных из-за загрязнения геномной ДНК.
Если праймеры не могут быть разработаны для разделения экзонов или экзон-экзонных границ, может потребоваться обработка образцов РНК ДНКазой I, не содержащей РНКазы, или двухцепочечной ДНКазой, чтобы удалить загрязнение геномной ДНК.
RT-qPCR контроль
Отрицательный контроль обратной транскрипции (контроль -RT) должен быть включен во все эксперименты RT-qPCR для обнаружения загрязнения ДНК (например, геномной ДНК или продуктов ПЦР из предыдущих реакций).Этот контроль содержит все компоненты реакции, кроме обратной транскриптазы.Поскольку с этим контролем обратной транскрипции не происходит, если наблюдается ПЦР-амплификация, наиболее вероятно загрязнение ДНК.
Время публикации: 02 августа 2022 г.








